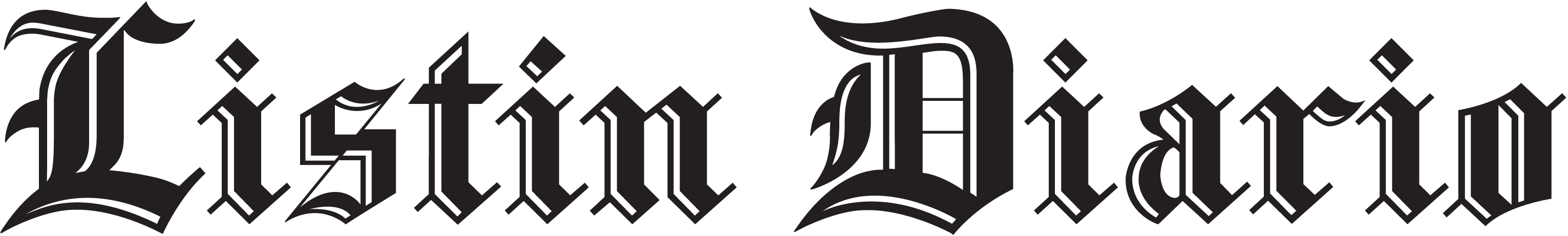País está en lista para recibir vacunas de Pfizer y Moderna
El especialista Marcos Espinal explicó que el portafolio del organismo incluye 10 vacunas que se encuentran en diferentes fases.
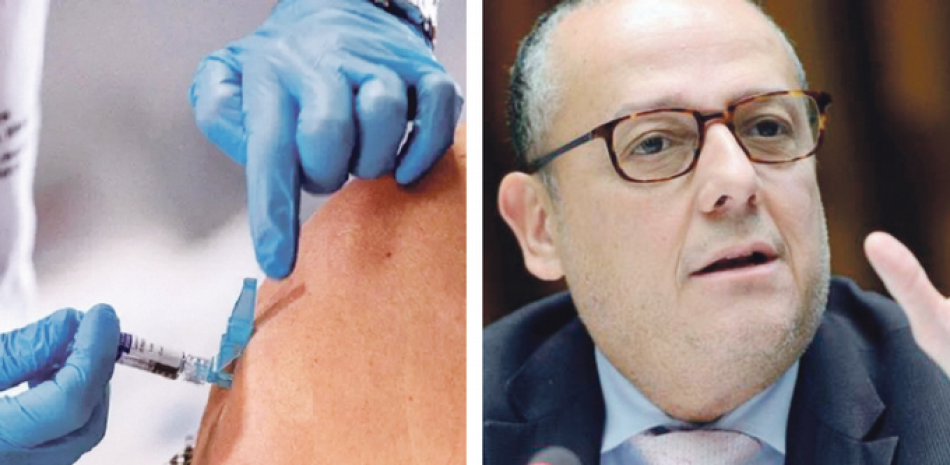
La OMS precalifica las vacunas y desarrolla normas y estándares internacionales, según explicó el especialista Marcos Espinal.
Ante el inicio ya de la aplicación en varios países de las vacunas contra el Covid-19 de Pfzer y Moderna, las dos primeras aprobadas de emergencia, la Organización Mundial de la Salud (OMS) y la Alianza Mundial de Vacunas (GAVI) iniciaron negociaciones para su inclusión a través del COVAX, que es el mecanismo al que la organización se ha adherido y en cuya lista de países inscritos figura República Dominicana.
Los detalles fueron dados a Listín Diario por el doctor Marcos Espinal, director del Departamento de enfermedades transmisibles y determinantes ambientales de OPS/OMS, quien dijo además que probable en las próximas semanas Astra Zeneca sea aprobada en algunos países, y que es en la que el país hizo un aporte económico inicial para estar en la lista de los primeros en recibirla una vez sea aprobada
No obstante Espinal, entrevistado vía correo electrónico, no especificó el avance de las negociaciones con las dos vacunas aprobadas para emergencia ni para qué fecha se podría estar distribuyendo a los países inscritos en el COVAX.
Recordó que las agencias internacionales no son reguladoras de los países y que la función de aprobar definitivamente una vacuna o para uso de emergencia corresponde a las agencias reguladoras de cada país (FDA en USA, ANVISA en Brasil, MHRA en Uk, COFEPRIS en México, etc.).
Explicó que la OMS precalifica las vacunas y desarrolla normas y estándares internacionales, de modo que los países de todo el mundo puedan regular los productos y tecnologías sanitarias de forma coherente.
Cadena de frío “Estamos en negociaciones para ver cómo se incluye a través del COVAX que es el mecanismo al que nos hemos adherido. Recuerda que el problema de esa vacuna (Pfizer) es que la mayoría de nuestros países no tienen disponibilidad de la cadena de frío que necesita esa vacuna y se deben buscar soluciones al respecto”, señaló.
Sobre la vacuna que elabora la empresa Astra Zeneca en colaboración con la universidad de Oxford, Espinal señaló que parece ser que tiene una eficacia de alrededor 70% lo que es aceptable para su uso, pero todavía no ha sido aprobada ya que hay algunas cosas que aclarar con respecto a la misma.
No obstante, agregó que se está trabajando para tratar de aumentar la eficacia de la misma un poco más y que es probable que en las próximas semanas Astra Zeneca sea aprobada en algunos países.
Sean seguras Espinal explicó que las agencias internacionales precalifican las vacunas y las agencias reguladoras nacionales aprueban para uso.
Destacó que la precalificación de la OMS garantiza que las vacunas utilizadas en los programas de inmunización sean seguras y eficaces, y además proporciona a los Estados miembros y otros socios la información necesaria para comprar vacunas que satisfagan las necesidades específicas del programa.
La OMS, agregó Espinal, también examina y comparte datos de vacunas sobre eficacia, potencia, termoestabilidad, presentación, etiquetado y condiciones de envío.
Agregó que para que una vacuna ingrese al proceso de precalificación de la OMS, la Autoridad (Agencia) Nacional Reguladora debe ser determinada como “funcional” de acuerdo con los indicadores del organismo.
CATÁLOGO El portafolio de COVAX. El portafolio actual de COVAX incluye 10 vacunas que son AstraZeneca/ University of Oxford (Phase 3); Clover Biopharmaceuticals, China (Phase 1);
CureVac, Germany (Phase 2B/3); Inovio, USA (Phase 2); Institut Pasteur/Merck/Themis, France/USA/Austria (Phase 1); Moderna, USA (Phase 3); Novavax, USA (Phase 3); SK bioscience, South Korea (Preclinical); University of Hong Kong, Hong Kong (Preclinical) y University of Queensland/ CSL, Australia (Phase 1, programme discontinued).