MALARIA VACUNA
La vacuna antimalaria de Oxford confirma su eficacia y seguridad en un ensayo en fase 3
La vacuna R21/Matrix-M se diseñó en 2011 como una mejora potencial de la RTS, S/AS01, diseñada en la década de 1980.
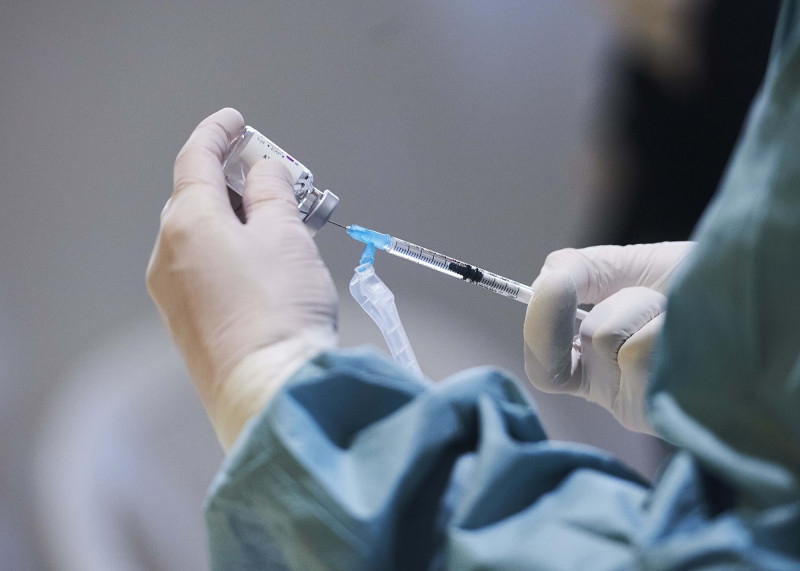
Vacunas.
La vacuna antipalúdica R21/Matrix-M confirmó "una alta" eficacia (78 % de media) y "un buen perfil" de seguridad en niños de 5 a 17 meses durante el primer año, según los datos de un nuevo ensayo clínico en fase 3 realizados en Burkina Faso, Kenia, Malí y Tanzania.
La vacuna R21/Matrix-M se diseñó en 2011 como una mejora potencial de la RTS, S/AS01, diseñada en la década de 1980.
El estudio en fase 3, cuyos resultados publica hoy Lancet, inmunizó a más de 4.800 niños y con él se constató una eficacia media de la vacuna del 78 % durante el primer año de seguimiento en todos los centros en el grupo de edad de 5 a 17 meses.
Ese es el grupo de edad en el que se estudian la mayoría de las vacunas contra la malaria, indicó en un comunicado la Universidad de Oxford, que ha desarrollado la vacuna y que fabrica Serum Institute de India.
La eficacia durante el periodo de un año fue muy similar en todos sitios donde se desarrollo el estudio y en diferentes entornos de transmisión.
Ninguna otra vacuna ha registrado una eficacia superior al 55 % en el mismo grupo de edad y, además, una dosis de refuerzo al año mantuvo una buena eficacia durante los 6-12 meses siguientes, agrega la nota.
La vacuna también redujo los índices de infección en niños a los 12 y 18 meses tras recibir el preparado, “lo que sugiere un efecto potencialmente beneficioso en la reducción de la transmisión de la malaria”.
Se observaron respuestas inmunitarias significativamente mayores a R21/Matrix-M y una eficacia ligeramente mayor en niños de 5 a 17 meses en comparación con las otras vacunas de 18 a 36 meses, "lo que respalda el despliegue planificado de la vacuna inicialmente a partir de los 5 meses de edad en niños africanos pequeños".
Los datos de seguridad del ensayo “han sido tranquilizadores”, al no producirse “acontecimientos adversos graves relacionados con la inmunización”, agrega la nota.
La vacuna fue bien tolerada, siendo el dolor en el punto de inyección y la fiebre los acontecimientos adversos más frecuentes, además no hubo muertes relacionadas con el tratamiento.
Los resultados de este ensayo en fase 3 han respaldado la aprobación reglamentaria y la concesión de licencias en varios países africanos, recuerda el comunicado.
La malaria es la principal causa de muerte entre niños africanos pequeños, con más de 600.000 fallecimientos cada año en todo el mundo.