SALUD
La vacuna contra el Covid-19 cada vez más cerca de quitarle la corona al virus
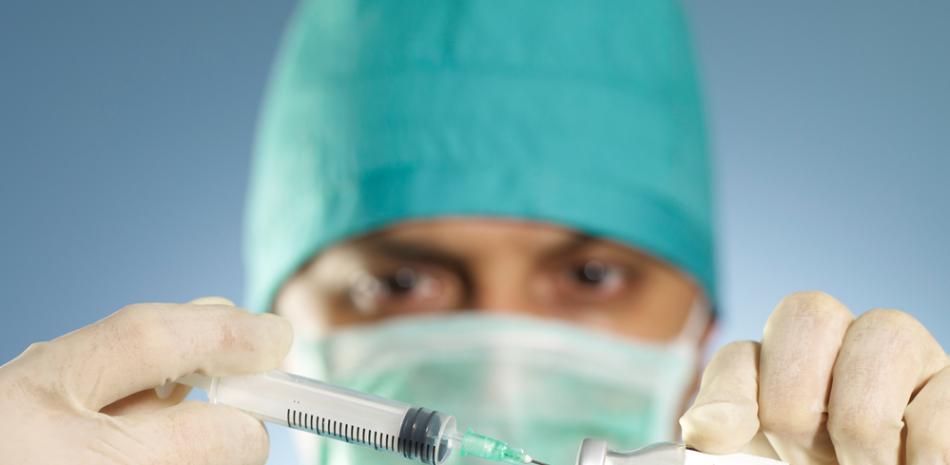
La humanidad pide a gritos una vacuna para prevenir el Covid-19. Hay científicos, laboratorios, universidades y firmas de todo el mundo que se han empleado a fondo para lograrla. Pero el hecho de que sea una necesidad imperiosa no compromete el cumplimiento que debe seguir su desarrollo para que dé una respuesta segura y eficaz a la situación creada por el virus.
Tatiana Deschamps, directora médica de Johnson & Johnson para Venezuela, Centro América y el Caribe tiene una buena noticia para aliviar un poco la carga de preocupación y miedo que tiene la población latina, donde cada vez hay más casos de muertes y de contagio. Se trata de que la fase 1/2a del ensayo clínico de su vacuna candidata para prevenir el Covid-19, iniciará en julio y no en septiembre como estaba previsto.
Estar en la la fase 1/2a del estudio significa que ya están en la etapa donde se pone a prueba la seguridad, los efectos secundarios y la mejor dosis de un tratamiento nuevo.
Los esfuerzos que hace la firma para acelerar el desarrollo y la producción de una vacuna contra el SARS-CoV-2 se han aumentado por la colaboración entre Janssen y la Autoridad de Investigación y Desarrollo Avanzado Biomédico (BARDA), parte de la Oficina del Secretario Asistente de Preparación y Respuesta (ASPR) en el Departamento de Salud y Servicios Humanos de Estados Unidos.
En respuesta a que cuáles son las fases por las que debe pasar una vacuna y en qué consiste cada una de ellas, Deschamps dijo que su desarrollo pasa por tres etapas. Las definió.
Etapa de evaluación antes de la utilización en seres humanos, en donde se evalúa si la vacuna candidata genera la protección que se necesita.
Primera etapa de evaluación en seres humanos, en donde se evalúa la seguridad y si la vacuna funciona en la prevención en una población más reducida.
Segunda etapa de evaluación en seres humanos, en donde se expande la cantidad de seres humanos expuestos a la vacuna, aumentando la evaluación de seguridad y eficacia de la misma.
El proceso Al hablar sobre el tiempo promedio que se toma el desarrollo de una vacuna, la especialista detalla que normalmente este proceso toma entre siete y ocho años, pero que en la firma para la que trabajase han dedicado de manera incansable junto a otras instituciones de salud, autoridades sanitarias y órganos internacionales para acelerar al máximo los tiempos, pero con la garantía de evaluar de manera eficiente la seguridad y eficacia de la vacuna candidata.
Comenta que la del SARS-CoV-2 que ellos desarrollan podría estar lista antes de lo acostumbrado porque cuentan con la experiencia en la utilización de su plataforma de desarrollo de vacunas. “Esto nos pone en una posición ideal para ayudar a responder a las necesidades de salud pública de nuestros tiempos. Esta plataforma ha permitido una reacción rápida para el desarrollo de otras terapias transformadoras, como fue el caso de la vacuna contra el Ébola. Esta misma experiencia la estamos aplicando para el desarrollo de vacunas candidatas contra otras necesidades apremiantes de nuestros tiempos, como lo es el HIV y el virus sincicial respiratorio”, explica.
Sobre la plataforma que disponen para el desarrollo de vacunas, Deschamps informa que tiene una capacidad de producción de varios millones de dosis, algo fundamental para responder a una pandemia. “La capacidad de producción de las dosis es tan importante cuanto la seguridad y eficacia de la vacuna. Sabemos que las necesidades de salud son globales y por eso estamos buscando activamente expandir aún más nuestra capacidad de producción en Europa y en otras geografías”, señala.
El costo de desarrollo Acerca de este tema, la directora médico de la referida firma, sostiene que el costo de una vacuna es muy variable y depende de varios factores. “En lo que a nosotros respecta, puedo decir que durante más de 130 años hemos buscado mantener con buena salud a personas de todas las edades y de todas las etapas de la vida enfocándonos más que todo en soluciones”, dice.
PREGUNTA Y RESPUESTA ¿Quién puede formar parte de un ensayo clínico de una vacuna? En el caso de la que están desarrollando ustedes, ¿dónde están, ¿cómo se seleccionan, reciben algún beneficio o es totalmente voluntario?
El ensayo clínico que iniciaremos a mediados de julio contará con la participación de más de 1,045 voluntarios sanos en Estados Unidos y Bélgica que se encuentran entre los 18 y 55 años y también con mayores de 65 años. Como en otros ensayos clínicos, la participación es siempre voluntaria y conducida de acuerdo con las guías internacionales para el desarrollo de este tipo de estudios. Así lo explica Deschamps, neumóloga, con alrededor de 15 años de experiencia en la industria farmacéutica.
En un contexto de pandemia como la actual, una vez encontrada una vacuna, ¿cómo se determina su distribución? ¿A quiénes se les debería administrar primero?
Considerando los números de casos en las distintas regiones del mundo sabemos que los niveles de transmisión son dinámicos. Tomando en cuenta que tendremos éxito en el desarrollo de la vacuna candidata, trabajaremos en conjunto con las organizaciones internacionales para garantizar que nuestras soluciones alcancen a todas las personas que las necesitan. Con este mismo objetivo estamos buscando activamente expandir nuestra capacidad de producción para apoyar a los esfuerzos del control de la pandemia.
¿Están las farmacéuticas en capacidad de producir una vacuna contra el SARS-CoV-2 para prácticamente todo el mundo?
Nosotros nos basamos en nuestra experiencia en la producción masiva de vacunas para garantizar la disponibilidad de mil millones de dosis de nuestra vacuna candidata durante 2021. Lo hemos hecho en el pasado, con el caso de la vacuna para el Ébola.
En paralelo a nuestros esfuerzos en desarrollar esta vacuna, estamos ampliando aún más nuestra capacidad de producción. Estamos trabajando incansablemente para cumplir con nuestro compromiso y objetivo de brindar una respuesta rápida, eficaz y segura ante la pandemia de coronavirus.