SALUD
Desarrollan un antibiótico que mata las bacterias y evita que surjan resistencias
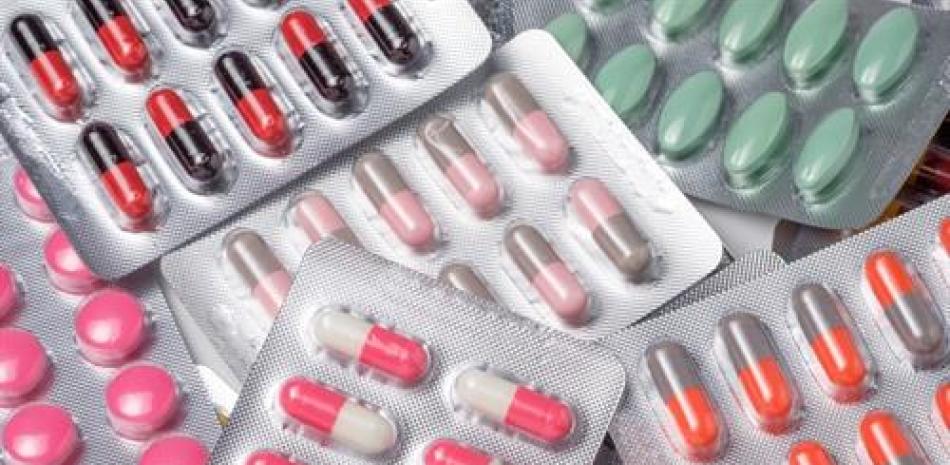
Seguir el consejo de completar el tratamiento con antibióticos puede poner en riesgo la salud. Fuente: Europa Press
Un equipo de investigadores de la Universidad de Princeton, en Estados Unidos han encontrado un compuesto, SCH-79797, que tiene un doble mecanismo ya que mata las bacterias Gram negativas y evita la resistencia a los medicamentos, según publica en la revista 'Cell'.
Las infecciones bacterianas tienen dos orígenes, las Gram-positivas y las Gram-negativas, llamadas así por el científico que descubrió cómo distinguirlas. La diferencia clave es que las bacterias gramnegativas están blindadas con una capa externa que evita la mayoría de los antibióticos. De hecho, no hay nuevas clases de medicamentos Gram-negativos que maten en el mercado en casi 30 años.
El nuevo compuesto eficaz con todo tipo de bacterias, desde 'E. coli' hasta MRSA (Staphylococcus aureus resistente a la meticilina), puede perforar simultáneamente las paredes bacterianas y destruir el ácido fólico dentro de sus células, a la vez que es inmune a la resistencia a los antibióticos.
"Este es el primer antibiótico que puede apuntar a Gram-positivos y Gram-negativos sin resistencia --explica Zemer Gitai, profesor de biología de Princeton y autor principal del artículo--. Pero lo que más nos entusiasma como científicos es algo que hemos descubierto sobre cómo funciona este antibiótico, atacando a través de dos mecanismos diferentes dentro de una molécula, que esperamos que sea generalizable, llevando a nuevos y mejores tipos de antibióticos en el futuro".
La mayor debilidad de los antibióticos es que las bacterias evolucionan rápidamente para resistirlos, pero el equipo de Princeton descubrió que incluso con un esfuerzo extraordinario, no pudieron generar resistencia a este compuesto. "Esto es realmente prometedor, por eso llamamos a los derivados del compuesto 'Irresistin'", asegura Gitai.
Lo consideran el santo grial de la investigación sobre antibióticos: un antibiótico que es efectivo contra enfermedades e inmune a la resistencia, a la vez que es seguro en humanos (a diferencia del alcohol o lejía, que son irresistiblemente fatales para las células humanas y las células bacterianas por igual).
Pero la irresistibilidad es una espada de doble filo. La investigación típica sobre antibióticos implica encontrar una molécula que pueda matar bacterias, criar varias generaciones hasta que la bacteria desarrolle resistencia a ella, observar cómo funciona exactamente esa resistencia y usarla para realizar ingeniería inversa de cómo funciona la molécula en primer lugar.
Pero como SCH-79797 es irresistible, los investigadores no tenían nada de lo que hacer ingeniería inversa. "Esta fue una verdadera hazaña técnica --asegura-- Gitai. Ninguna resistencia es una ventaja del lado del uso, sino un desafío del lado científico".
El equipo de investigación tuvo dos enormes desafíos técnicos: tratar de probar lo negativo (que nada puede resistir a SCH-79797) y luego descubrir cómo funciona el compuesto.
Para demostrar su resistencia a la resistencia, el graduado en doctorado James Martin probó infinitos ensayos y métodos diferentes, ninguno de los cuales reveló una partícula de resistencia al compuesto SCH. Finalmente, probó la fuerza bruta: durante 25 días expuso las bacterias al fármaco una y otra vez. Como las bacterias tardan unos 20 minutos por generación, los gérmenes tenían millones de posibilidades de desarrollar resistencia, pero no lo hicieron. Para verificar sus métodos, el equipo también pasó en serie otros antibióticos (novobiocina, trimetoprima, nisina y gentamicina) y rápidamente generaron resistencia a ellos.
También intentaron usarlo contra especies bacterianas que son conocidas por su resistencia a los antibióticos, incluida 'Neisseria gonorrhoeae', que se encuentra en la lista de las 5 principales amenazas urgentes publicada por el Centro para el Control y Prevención de Enfermedades.
"La gonorrea plantea un gran problema con respecto a la resistencia a múltiples fármacos --recuerda Gitai--. Nos hemos quedado sin medicamentos para la gonorrea. Con la mayoría de las infecciones comunes, los medicamentos genéricos de la vieja escuela aún funcionan, pero no para la gonorrea".
Los investigadores incluso obtuvieron una muestra de la cepa más resistente de 'N. gonorrhoeae' de la Organización Mundial de la Salud, una cepa que es resistente a todos los antibióticos conocidos y también acabó con ella. "Estamos bastante entusiasmados con eso", reconoce.
Sin resistencia a la ingeniería inversa, los investigadores pasaron años tratando de determinar cómo la molécula mata las bacterias, utilizando una gran variedad de enfoques, desde técnicas clásicas que han existido desde el descubrimiento de la penicilina hasta la tecnología punta.
Finalmente comprobaron que SCH-79797 usa dos mecanismos distintos dentro de una molécula, como una flecha cubierta de veneno.
"La flecha tiene que ser aguda para introducir el veneno, pero el veneno también tiene que matar por sí solo", explica Benjamin Bratton, investigador asociado en biología molecular y profesor en el Instituto Lewis Sigler de Genómica Integrativa, otro coprimer autor.
La flecha apunta a la membrana externa, atravesando incluso la gruesa armadura de las bacterias Gram negativas, mientras que el veneno destruye el folato, un componente fundamental del ARN y el ADN. Los investigadores se sorprendieron al descubrir que los dos mecanismos funcionan sinérgicamente, combinándose en más de una suma de sus partes.
"Si solo tomas esas dos mitades, hay medicamentos disponibles comercialmente que pueden atacar a cualquiera de esas dos vías, y simplemente los arrojas a la misma olla, eso no mata tan efectivamente como nuestra molécula, que los ha unido juntos en el mismo cuerpo ", apunta Bratton.
Pero había un problema: el SCH-79797 original eliminó células humanas y células bacterianas a niveles más o menos similares, lo que significa que, como medicamento, corría el riesgo de matar al paciente antes de matar la infección.
Una derivada 'Irresistin-16' arregló eso. Es casi 1.000 veces más potente contra las bacterias que las células humanas, por lo que es un antibiótico prometedor. Como confirmación final, los investigadores demostraron que podían usar Irresistin-16 para curar ratones infectados con 'N. gonorrhoeae'.
Este paradigma de flecha envenenada podría revolucionar el desarrollo de antibióticos, señala KC Huang, profesor de bioingeniería y de microbiología e inmunología en la Universidad de Stanford que no participó en esta investigación.
Huang, que fue investigador postdoctoral en Princeton asegura que "este compuesto ya es tan útil por sí mismo, pero también, las personas pueden comience a diseñar nuevos compuestos inspirados en esto. Eso es lo que ha hecho que este trabajo sea tan emocionante".
En particular, cada uno de los dos mecanismos, la 'flecha' y el 'veneno', se dirigen a procesos que están presentes tanto en bacterias como en células de mamíferos. El folato es vital para los mamíferos (razón por la cual se les dice a las mujeres embarazadas que tomen ácido fólico) y, por supuesto, tanto las bacterias como las células de los mamíferos tienen membranas.
"Un estudio como este dice que podemos volver atrás y revisar lo que pensamos que eran las limitaciones en nuestro desarrollo de nuevos antibióticos --apunta Huang--. Desde el punto de vista social, es fantástico tener nuevas esperanzas para el futuro".