Salud Pública prohíbe importar y comercializar pruebas rápidas de Covid-19 a partir del 1 de febrero
SOLO PERMITIRÁN LAS QUE TENGAN EL REGISTRO SANITARIO QUE EMITE LA DIGEMAPS
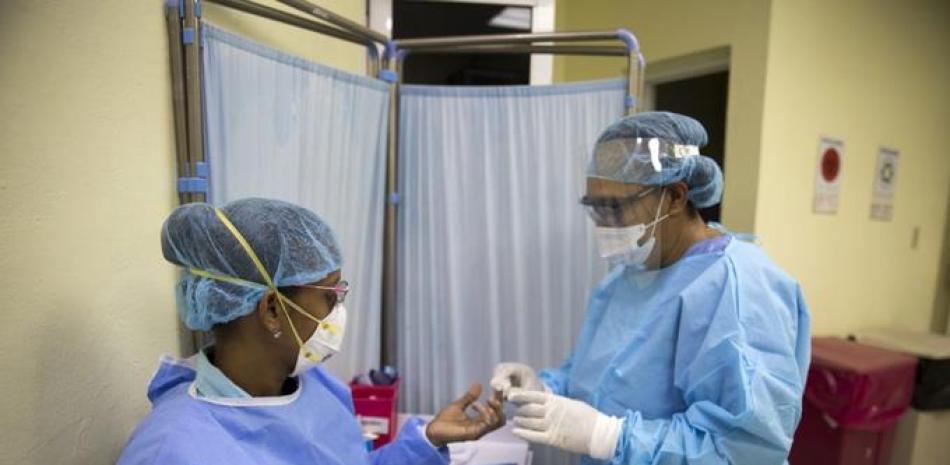
El Ministerio de Salud Pública advirtió este miércoles que a partir del primero de febrero no se permitirá la importación y comercialización de pruebas rápidas para detectar el covid-19, sin contar con la debida certificación de registro sanitario.
En un espacio pagado, el Ministerio de Salud, bajo la firma del ministro Plutarco Arias, llama a las empresas y al público en general a abstenerse de comercializar esas pruebas rápida de detección de anticuerpo del covid-19, en cualquiera de sus presentaciones, si no cuentan con la aprobación de ese Ministerio a través de una certificación de registro sanitario obligatorio que emite la Dirección General de Medicamentos, Alimentos y Productos Sanitarios (Digemaps).
“Por lo tanto, a partir de la fecha de publicación del presente aviso y hasta la fecha indicada, solo será autorizada una última importación para una cantidad máxima de cinco mil cajas por distribuidor debidamente registrado ante la Digemaps”.
Este aviso fue emitido este miercoles cuando en el país hay una gran demanda de pruebas de coronavirus, dado el incremento de casos que se registran y la gran demanda hospitalaria de pacientes afectados por covid-19.
Ayer martes se reportaron 475 nuevos casos y 1,063 personas hospitalizadas, de las que 281 están en Unidades de Cuidados Intensivos.